Дальнейшую конверсию вермелона в черное вещество могли осуществлять уже и brm-1-, и brm-2-, и aim-мутанты. Отсюда было сделано заключение о реальности протекания этой после- довательности реакций in vivo, и вермелон стал рассматриваться как последний (терминальный) кетон на пути от (+)-сциталона к меланину.
При этом полагали, что он дегидрируется в 1,8-диоксинафталин. Во всяком случае, при инкубации (-)-вермелона с alm-1 удалось выделить нафтол, идентичный по хроматографическим и спектральным характеристикам именно этому соединению. Наиболее приемлемым объяснением отсутствия у мутанта brm-1 ферментативной активности, необходимой для превращения любого из биосинтетических 3-окситетралонов в соответствующий нафтол, авторы считают предположение об одноферментном катализе обеих реакций дегидратации в конверсии (+)-сциталона в 1,8-ди- оксинафталин [Stipanovic, Bell, 1976]. Весь же путь от (+)-сциталона до меланина требует, по мнению авторов, участия не менее трех различных ферментов: дегидратазы, катализирующей превращение (+)-сциталона в 1, 3, 8-триоксинафталин и вермелона в 1,8-диоксинафталин; алкогольде- гидрогеназы, восстанавливающей 1, 3, 8-триоксинафталин в вермелон, и оксидазы, окисляющей 1,8-диоксинафталин в продукты, полимеризующиеся в дальнейшем в меланин. Последний фермент кажется авторам, вероятнее всего, лакказой (на том основании, что именно она осуществляет эту реакцию у грибов-макромицетов).
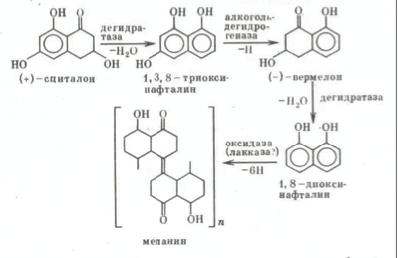
Общая схема синтеза меланина у V. dahliae, следовательно, должка выглядеть так [Bell et al., 1976с].
В соответствии с ней предположено, что у мутанта brm-1 отсутствует дегидратаза, мутант brm-2 лишен алкогольдегидрогеназы, а мутанты типа aim имеют генетический блок в биосинтезе исходного субстрата — (+)-сциталона.